營養與代謝 |犬隻胃擴張扭轉之內源性生物學最新發現
重點摘要
犬隻胃擴張扭轉(Gastric Dilatation-Volvulus, GDV)長期被視為因解剖結構或餵食習慣引發的急性物理性急症。然而,當代國際獸醫研究揭示了該病更深層的生物學基礎:腸道微生態失衡(Dysbiosis)與遺傳易感基因的交互作用。研究證實,GDV 患犬體內存在顯著的菌叢偏移,特別是促發炎微生物「柯林斯氏菌」(Collinsella)的異常擴張,這與犬隻的遺傳缺陷密切相關 。這種失衡導致腸道內異常發酵產生大量氣體並觸發全身性發炎,而非單純的吞入空氣。
從物理特徵到分子機制:胃擴張扭轉的新發現
胃擴張扭轉(GDV)是一種在大型及巨型深胸犬種中進展極快且危及生命的臨床症候群 。傳統上,獸醫界與飼主多將目光鎖定在環境因素,如單次大量攝食、進食後劇烈運動、或高架餵食器的使用 。然而,即便嚴格控管這些外部變數,GDV 的發生率依然居高不下,這促使科學家轉向探索犬隻內部的生物學特徵。
最新的同行評議研究,特別是針對大丹犬(Great Danes)的大規模微生態分析發現,GDV 並非隨機發生的物理意外,而是一種具備深厚生物學背景的複雜疾病 。研究顯示,GDV 患犬的腸道內環境與健康犬隻有著本質上的差異。這種差異不僅體現在患病當下的急性期,甚至在發病前的潛伏期,其菌叢結構便已展現出獨特的「風險特徵」 。
根據一項發表於《PLOS One》的關鍵研究,科學家對 38 隻健康大丹犬與 37 隻曾發生 GDV 的大丹犬進行了 16S rRNA 基因定序分析 。結果令人意外:GDV 患犬的糞便微生物群展現出更高的 alpha 多樣性。在人類醫學中,較高的多樣性通常與健康掛鉤,但在犬隻 GDV 的背景下,這種「異常多樣性」反映了稀有、潛在致病性微生物的無序擴張,打破了原本由少數核心菌屬維持的穩態 。
腸道微生態的「風險特徵」:關鍵菌屬的此消彼長
在微生物門(Phylum)的水平上,GDV 犬隻表現出明顯的分類學偏移。這種偏移被認為是導致胃部過度發酵與腸道屏障功能受損的核心誘因 。
| 微生物分類指標 | 健康犬隻特徵 | GDV 患犬特徵 | 生物學意義 |
|---|---|---|---|
| 擬桿菌門 (Bacteroidetes) | 豐度較高 (約 63%) | 顯著下降 (約 48%) | 影響碳水化合物的穩定降解 |
| 厚壁菌門 (Firmicutes) | 豐度適中 (約 26%) | 顯著升高 (約 39%) | 與能量攝取過剩及特定發酵路徑相關 |
| 放線菌門 (Actinobacteria) | 極低豐富度 (約 0.14%) | 異常擴張 (約 0.49%) | 包含關鍵促發炎菌屬如柯林斯氏菌 |
| 變形菌門 (Proteobacteria) | 低水平維持 | 呈現上升趨勢 | 常見於腸道發炎與菌叢失調 |
在具體的屬(Genus)水平上,柯林斯氏菌(Collinsella)的崛起最受學界矚目 。研究數據顯示,該菌屬在 GDV 患犬中的水平顯著升高。這與人類醫學中對發炎性腸病(IBD)、類風濕性關節炎以及動脈粥狀硬化的研究結果不謀而合 。

柯林斯氏菌的促發炎機制與氣體代謝
柯林斯氏菌並非僅僅是菌叢失衡的「旁觀者」,它在病理過程中扮演著「驅動者」的角色 。
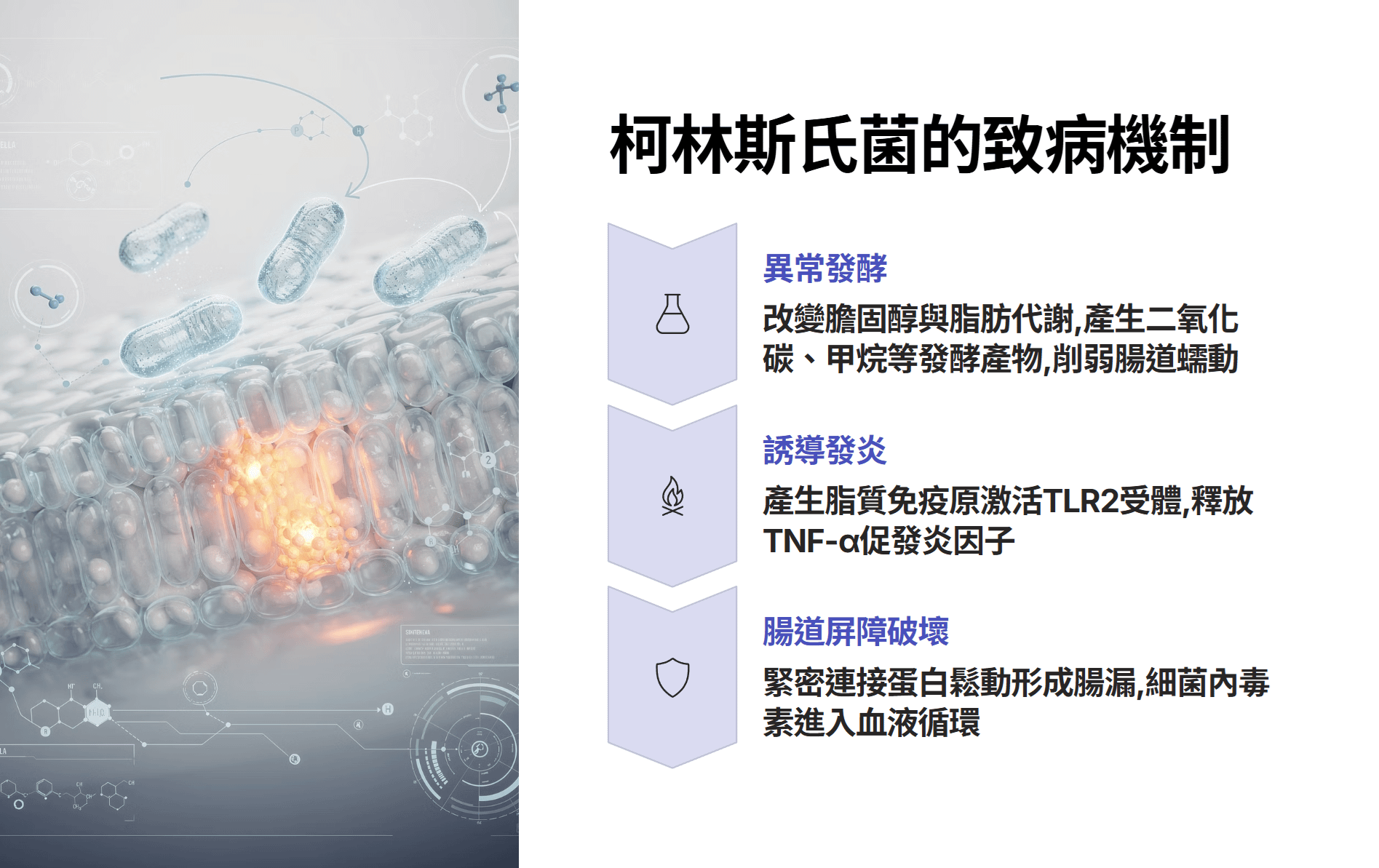
第一,代謝與發酵:柯林斯氏菌能改變宿主腸道內的膽固醇與脂肪代謝。更重要的是,它參與了異常的發酵路徑,產生的代謝產物可能削弱腸道蠕動,並促使氣體迅速積聚 。化學分析顯示,GDV 胃內積聚的氣體並非來自吞嚥的大氣,而是充滿了二氧化碳、甲烷等典型的微生物發酵產物 。
第二,誘導全身性發炎:研究發現柯林斯氏菌(如 Collinsella aerofaciens)能產生一種特定的脂質免疫原。這種物質能直接激活宿主先天免疫系統中的「類鐸受體 2」(TLR2),進而觸發樹突狀細胞釋放強效促發炎細胞因子,如腫瘤壞死因子-α(TNF-α) 。這種慢性低度發炎會導致腸道黏膜的「緊密連接蛋白」(Tight Junctions)鬆動,形成腸漏(Leaky Gut),讓細菌內毒素進入血液循環,進一步惡化犬隻的健康狀態,降低其對急性的胃擴張應激的承受力 。
遺傳基因與菌群的交叉對話:TLR5 的關鍵角色
GDV 的一個核心謎團是:為什麼在同樣的飲食條件下,某些犬隻會發病而其他則不會?答案隱藏在犬隻的基因組中。研究鑑定出多個與 GDV 易感性相關的免疫系統等位基因 。
類鐸受體 5 (TLR5):TLR5 負責識別細菌的鞭毛蛋白(Flagellin)。在 GDV 高風險犬隻中,研究人員發現了特定的 TLR5 基因變異。當 TLR5 功能異常時,宿主的免疫系統無法有效監控和限制某些特定微生物(如柯林斯氏菌)的過度生長 。
這意味著,GDV 的風險是遺傳預設的。遺傳缺陷導致免疫系統對腸道菌群的管束力下降,進而引發微生態失衡;而這種失衡在特定的環境誘因下,最終導致了急性發病 。

發炎性腸病 (IBD) 與 GDV 的病理鏈結
臨床統計發現,患有發炎性腸病(IBD)的犬隻,發生 GDV 的機率顯著高於健康犬隻 。這並非巧合,因為兩者共享了相似的微生物與免疫學特徵。
在 IBD 犬隻中,柯林斯氏菌亦被觀察到是粘膜免疫反應的主要攻擊目標。研究發現,IBD 犬隻腸道內的免疫球蛋白 G(IgG)和免疫球蛋白 A(IgA)會優先與柯林斯氏菌結合,這表明該菌屬被免疫系統識別為具威脅性的入侵者,並觸發強烈的局部發炎反應 。對於寵物食品業者而言,這是一個重要的切入點:任何旨在緩解腸道發炎、改善 IBD 的營養策略,本質上都有助於降低 GDV 的長期風險 。
寵物食品產業的轉型:從「避坑」到「機能調節」
面對 GDV 的生物學真相,寵物食品產業的產品開發策略正在發生轉型。業者不再僅僅強調「低纖維」或「避開穀物」,而是轉向更為精準的營養介入 。
1. 益生元 (Prebiotics) 的精準篩選
益生元是能被有益菌選擇性利用的纖維底物 。針對 GDV 風險犬隻,業者可以引入如菊苣纖維(Inulin)、寡糖(FOS/MOS)等成分。這些成分能刺激擬桿菌屬與乳酸桿菌屬(Lactobacillus)的生長,並透過競爭排斥作用限制柯林斯氏菌的生存空間 。
2. 後生元 (Postbiotics) 與代謝調節
後生元是指滅活的微生物及其代謝產物,具備更高的加工穩定性,極適合添加到乾糧噴塗工藝中 。關鍵的後生元包括短鏈脂肪酸(SCFA),特別是丁酸鹽(Butyrate)。
強化屏障:丁酸鹽能為腸道上皮細胞提供能量,修復受損的緊密連接蛋白,防止細菌內毒素易位 。
抗炎特性:丁酸鹽能調節 T 細胞反應,抑制促發炎細胞因子的產生,從而緩解與遺傳易感性相關的慢性發炎 。
3. 個性化營養與微生態檢測
隨者 DNA 測序成本的下降,業者已開始推出居家腸道微生態分析套件 。
數據驅動配方:透過檢測犬隻體內的柯林斯氏菌丰度或擬桿菌/厚壁菌比例,業者可以為飼主提供定製化的營養建議,例如推薦富含抗炎 Omega-3 脂肪酸、特定益生菌株或高消化率蛋白質的配方,實現精準預防 。

生物學機制下的餵食行為管理
儘管內部生物學是基礎,但餵食行為依然是觸發急性扭轉的最後一根稻草。科學研究與業者專欄應持續強調以下幾點行為建議:
少量多餐:每日分 2-3 次餵食,可減少胃部的體積負荷與短時間內的發酵壓力 。
控制進食速度:慢食碗或益智餵食器的使用,能顯著降低吞氣症(Aerophagia)的發生,並減少因急性飽脹引發的胃蠕動功能障礙 。
地面餵食:最新的研究 對於高架餵食能防脹氣有了疑問,事實上反而發現高架餵食可能增加大型犬的風險,因此建議回歸地面餵食 。
總結與前瞻
犬隻胃擴張扭轉(GDV)的成因是多維度的,遺傳易感性(基因)、腸道微生態(細菌)與環境因素(飲食與壓力)在此交織 。柯林斯氏菌的升高與 TLR5 基因的變異,為我們提供了全新的干預靶點。
對於寵物食品業者而言,這不僅是挑戰,更是將科學研發實力轉化為市場領先優勢的機會。透過深耕「腸道-免疫-遺傳」軸的研發,我們可以開發出不僅能填飽肚子,更能從分子層面守護犬隻生命的劃時代產品。未來的寵物營養將不再是通用的公式,而是基於生物學數據的精準照護 。
給業者的 Tips:機能性預防配方與市場策略
優化腸道微生態平衡:在針對大型犬的配方中,優先選用高品質的動物蛋白與精準比例的益生元(如 FOS/MOS、菊苣纖維)。這有助於維持擬桿菌門的豐度,並透過競爭機制抑制如「柯林斯氏菌」等促發炎菌屬的擴張 。
引入後生元與穩定代謝產物:考量到乾糧加工中的高溫高壓環境,業者應評估添加熱穩定性高的「後生元」(如丁酸鈉)。丁酸鹽能有效修復腸道屏障(緊密連接蛋白),降低全身性發炎,從生物學底層增強犬隻對 GDV 的抵抗力 。
抗炎營養素的整合應用:在高風險犬種(如大丹犬、聖伯納犬)的配方中,增加 Omega-3 脂肪酸(如魚油或藻油)的水平。抗炎營養素能協同免疫系統調節,減緩由特定菌叢引發的慢性低度發炎反應 。
產品顆粒結構與物理管理:結合包裝上的「慢食教育」,引導飼主將產品與適當的餵食工具搭配使用 。
推動微生態檢測與個性化服務:與生物技術公司合作,推廣居家腸道健康檢測。透過數據分析,為飼主提供階段性的營養調整方案,將產品從「一次性購買」轉化為「長期的健康管理解決方案」 。
標籤透明化與科學背書:在標籤上明確列出所使用的特定益生菌或益生元種類,並在行銷中引用如同行評審的研究成果。現代飼主高度依賴數據與權威研究,科學透明度是建立高階品牌信任的核心 。
關注心理壓力的間接影響:研發具備緩解焦慮功能的成分(如茶胺酸或色胺酸),因犬隻的緊張情緒與腸道蠕動障礙及菌叢偏移高度相關。從「腸-腦軸」的角度全面預防 GDV 的觸發 。
資料來源:
Hullar, M. A. J., Lampe, J. W., Torok-Storb, B. J., & Harkey, M. A. (2018). The canine gut microbiome is associated with higher risk of gastric dilatation-volvulus and high risk genetic variants of the immune system. PLOS ONE, 13(6), Article e0197686.
Acton, S. M., et al. (2024). Full-length 16S rRNA gene sequencing reveals a core microbiome in the pet dog. Frontiers in Veterinary Science, 11, 1405470.
Salminen, S., et al. (2021). The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics. Nature Reviews Gastroenterology & Hepatology, 18(9), 649–667.
Moro, A., et al. (2025). Effects of postbiotic administration on canine health: A systematic review and meta-analysis. Microorganisms, 13(7), 1572.
Sharp, C. R., Rozanski, E. A., Finn, E., & Borrego, E. J. (2020). The pattern of mortality in dogs with gastric dilatation and volvulus. Journal of Veterinary Emergency and Critical Care, 30(3), 232–238.




